随着“仿制药质量和疗效一致性评价”政策的出台,临床试验的关注度不断提高。药物临床试验登记平台的数据也逐年增加,截止2018年4月27日,平台获得CTR号的临床试验8133项,其中公示5621项。
1、BE临床登记数量统计。
通过统计2016年至2018年包含所有“生物等效性/生物利用度”临床试验(这里试验目的不全部是一致性评价),截止2018年4月27日共计1092条,包含300多个药品的BE试验。下图为各月的BE临床登记数量统计图,从该图可以看出,随着仿制药一致性评价的开展,BE临床新登记数量从2016年8月开始保持一个较高数量,从侧面反映出一致性评价正在加速。

2、BE临床登记试验状态统计。
试验状态方面,对1092条BE临床登记进行分析,发现412条临床试验已经完成,占比38%;另外有23条是企业因为某些原因主动暂停了试验,其中一些原因比较有意思,如登记号CTR20171313主动暂停的原因是:总局于2017年12月29日公布西安杨森原研地产利培酮片为参比制剂,故不需额外开展此项研究。
3、BE临床登记最受关注的药品TOP10。
对BE临床登记试验的药品情况统计发现,2016年至2018年4月最受关注的药品为苯磺酸氨氯地平片,BE试验达到30个;其次是富马酸替诺福韦二吡呋酯片、他达那非片和阿莫西林胶囊。江苏黄河药业股份有限公司的苯磺酸氨氯地平片已经通过一致性评价;另外最受关注的TOP10药品中富马酸替诺福韦二吡呋酯片、阿莫西林胶囊、吉非替尼片,硫酸氢氯吡格雷片、瑞舒伐他汀钙片均已经有通过一致性评价的企业。
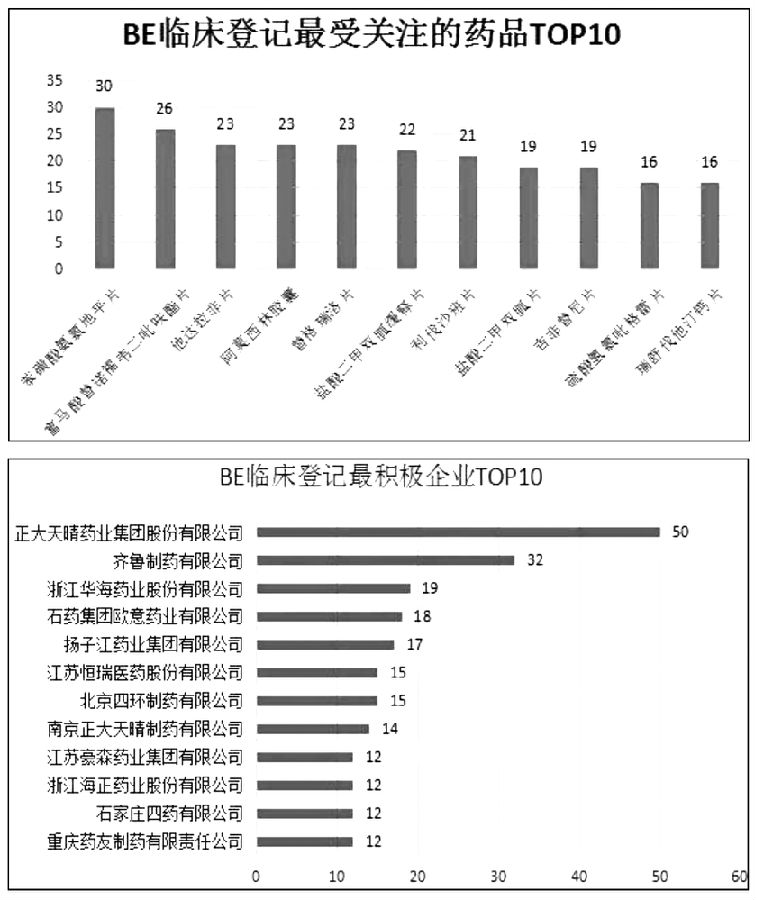
4、BE临床登记最积极的企业。
总的来说,2016至2018年4月BE临床登记数量和各企业的整体实力成正相关。正大天晴药业集团股份有限公司登记数量最多,登记号达到50个,旗下南京正大天晴制药有限公司还有14个登记号;其次是齐鲁制药有限公司。TOP10企业几乎为国内大型药企,可见,大型药企对仿制药质量和疗效一致性评价的重视度更高,且表现出较强的实力。
5、BE临床登记最受欢迎的临床试验机构。
随着生物等效性试验的开展,临床试验机构显得特别紧张,也成为了CRO公司和各药企争相合作的对象。2017年9月1日,国家食品药品监督管理总局、国家卫生和计划生育委员会联合发布了关于药物临床试验机构开展人体生物等效性试验的公告(2017年第119号),公告指出:根据《中华人民共和国药品管理法》《药物临床试验机构资格认定办法(试行)》的有关规定,药品监督管理部门会同卫生行政部门已经认定具有药物临床试验机构资格的医疗机构619家。经认定的药物临床试验机构均可以开展人体生物等效性试验。公告其他内容这里就不赘述了,感兴趣的朋友可以到原食药监总局网站查看。
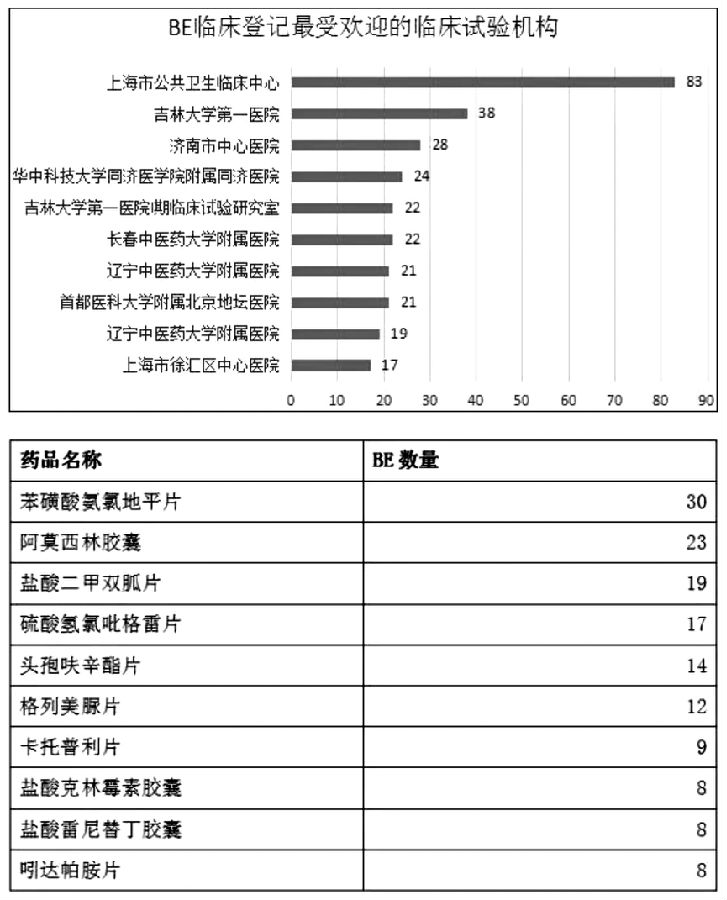
2016至2018年4月BE临床登记中最受欢迎的临床试验机构TOP10。其中上海市公共卫生临床中心最受欢迎,达到83个登记号,仔细分析发现其2018年的临床登记号就有36个。从地域来看,最受欢迎的临床机构大多在东部地区和东北地区。
6、289目录BE临床登记情况分析。
想必读者也想知道289目录药品的情况。数据显示,2016年至2018年4月BE临床新登记数量中,属于289目录的登记号为293条,占整体1092个登记号的26.8%,即便除去不是一致性评价的BE试验,占比仍不高。另外一方面,293条登记号中289目录中的药品仅73个,整体来说关注度还是不够。不过,289目录还有120多个药品的参比制剂还未确定,企业自然不会着急开展BE试验,毕竟BE试验费用不低,不容有误。
下表简单罗列了289目录BE临床登记最受欢迎的药品,这里就不做详细分析。
总的来说,仿制药一致性评价无疑是近3年圈内最热门的话题,而溶出度、BE试验又是一致性评价的关键。随着复杂注射剂一致性评价的开展,BE试验的关注度仍会很高。本文数据来源于药智中国临床试验数据库和药物临床试验登记与信息公示平台。
(选自《药智网》)